Het belang van het beschermen van uw steriliteitstestproces
Gedurende het productieproces worden productmonsters genomen en getest op microbiële besmetting. In de meeste gevallen zal de steriliteitstest aantonen dat het product vrij is van besmetting, waarna het product kan worden verzonden. Wanneer de resultaten aantonen dat het product besmet is, wordt de levering stopgezet om te voorkomen dat patiënten worden blootgesteld aan potentieel risico.
Als uw steriliteitsproces niet op de juiste manier is beschermd, kan besmetting vanuit de omgeving de test beïnvloeden en aangeven dat het product besmet is, terwijl dat niet het geval is. Dit kan leiden tot aanzienlijke kosten voor de fabrikant en mogelijk tot een tekort aan medicijnen voor patiënten als de partij moet worden afgekeurd. Bescherm het steriliteitstestproces tegen besmetting in de omgeving en verklein zo het risico op vals-positieve resultaten.
Ongeacht of uw methodologie membraanfiltratie of directe inoculatie is, een isolator kan duidelijke voordelen bieden.

Ontdek onze isolator voor steriliteitstesten
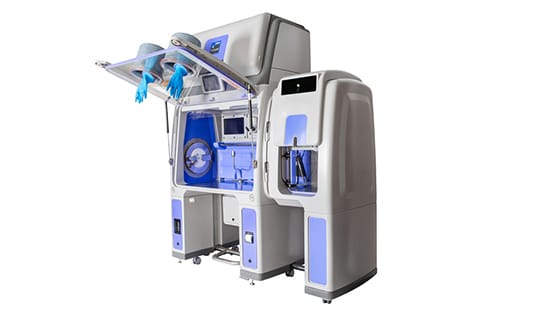
Bioquell Qube van Ecolab biedt een aseptische ISO 5 / klasse A-omgeving en omvat geïntegreerde Bioquell waterstofperoxidedamp-technologie, waarmee een gevalideerde 5-log sporendodende werking op blootgestelde oppervlakken binnen operationele gebieden wordt bereikt. Van de polymeer vormgeving tot de integratie met de Merck Millipore Sumbio Flex steriliteitspomp is de Bioquell Qube werkelijk uniek en een ideale oplossing voor steriliteitstesten.
*Bij gebruik volgens de instructies op het etiket werken Ecolab Bioquell-systemen met het Bioquell waterstofperoxide-sterilisatiemiddel-AQ (EPA registratienummer:1677-277)
Is een isolator de juiste keuze voor u? Heeft u de juiste isolator?
Wat zou een vals-positief of probleem voor u betekenen?
Het stilleggen van de productie vanwege een vals-positief resultaat kan leiden tot aanzienlijke uitvaltijd, onnodig schrappen van producten, tekorten aan medicijnen en mogelijk ook tot een slechtere positie van een bedrijf op de markt. Bovendien moet er rekening worden gehouden met de extra tijd, arbeid en kosten die voortvloeien uit CAPA-gerelateerde stappen.
Hoeveel cleanroom-ruimte vereist het proces?
Cleanroom-ruimte moet doorgaans worden geoptimaliseerd, omdat de prijs per vierkante meter voor het bouwen en exploiteren van de ruimte hoog kan zijn. Een isolator als de Bioquell Qube heeft een kleine voetafdruk die zelfs indien nodig eenvoudig kan worden verplaatst, vereist geen constructie en is geschikt voor gebruik in lager geclassificeerde gebieden. Voor specificaties kunt u contact opnemen met Ecolab.
Heeft uw steriliteitstestproces een klasse B-cleanroom nodig?
Met isolators kunt u testen in lager geclassificeerde cleanrooms uitvoeren, waar minder of geen kledingvoorschriften gelden. Bovendien kan waardevolle cleanroomruimte worden behouden voor andere essentiele activiteiten en kunnen de bedrijfskosten worden verlaagd, omdat hoger geclassificeerde cleanrooms grotere financiële investeringen in energie- en onderhoudskosten vereisen.
Is uw huidige proces gevalideerd en werkelijk herhaalbaar?
Geautomatiseerde bio-decontaminatie van binnenkomende materialen is een gevalideerd proces dat bij elke cyclus dezelfde doeltreffendheid garandeert. Dit helpt om het risico op een vals-positief resultaat verder te verkleinen.
Hoeveel steriliteitstesten moet u op één dag uitvoeren?
Cleanroom-ruimte moet doorgaans worden geoptimaliseerd, omdat de prijs per vierkante meter voor het bouwen en exploiteren van de ruimte hoog kan zijn. Een isolator als de Bioquell Qube heeft een kleine voetafdruk die zelfs indien nodig eenvoudig verplaatst kan worden, vereist geen constructie en is geschikt voor gebruik in lager geclassificeerde gebieden De Bioquell Qube kan bijvoorbeeld tot wel 60 testen per dag doen, afhankelijk van de configuratie. Voor specificaties kunt u contact opnemen met Ecolab.
Besteedt u uw steriliteitstestproces uit?
Er zijn voordelen verbonden aan het in eigen beheer uitvoeren van het proces, zoals meer controle, kostenbesparingen op de lange termijn en snellere resultaten. Door een isolator te selecteren die in CNC-ruimtes of lager geclassificeerde cleanrooms kan worden geplaatst, wordt dit voor bedrijven werkelijkheid, ondanks de initiële kosten voor de apparatuur.

De impact van afkeuring
De impact van een afgekeurde test kan voor een farmaceutische fabrikant aanzienlijk zijn, omdat dit doorgaans resulteert in:
- Het uitstellen van de vrijgave en mogelijk schrappen van de partij van het product die de test niet heeft doorstaan
- Extra reiniging en desinfectie van productieruimtes
- Betrokkenheid van regelgevende instantie
- Financiële verliezen voor de fabrikant
- Tijdrovende onderzoeken uitvoeren
- Medicijntekort voor patiënten
- Het stilleggen van de productie van het product terwijl er onderzoeken worden uitgevoerd
Dat steriliteitstests resulteren in afkeuring wordt echter niet altijd veroorzaakt door besmetting van het product.
Een vals-positief resultaat kan ontstaan als verontreiniging vanuit de omgeving of via de uitvoerende operator in de test terechtkomt en een fout oplevert. Een product wordt als besmet beschouwd, terwijl het in werkelijkheid geen schadelijke micro-organismen bevat.
In geval van afkeuring bij een steriliteitstest ligt de bewijslast bij de fabrikant. Die moet aantonen dat de afkeuring het gevolg is van besmetting door de gebruiker en/of de laboratoriumomgeving en dat is moeilijk te bewijzen. Hierdoor leiden vals-positieve resultaten er vaak toe dat conforme en effectieve producten worden vernietigd.
Bescherm uw bedrijf met een isolator voor steriliteitstesten

Regelgevende richtlijnen voor isolators:
- In EU GMP Bijlage 1 sectie 10.6 staat:
"De steriliteitstest moet worden uitgevoerd onder aseptische omstandigheden."
- De richtlijnen van de FDA voor de industrie voor steriele geneesmiddelenproducten die worden geproduceerd via aseptische verwerking gaan nog een stap verder en stellen in sectie XI:
"Het gebruik van isolatoren voor steriliteitstesten minimaliseert de kans op een vals positief testresultaat."
- Volgens EU GMP-bijlage 1 is een isolator:
"Een behuizing waarin reproduceerbare interne bio-decontaminatie plaatsvindt, met een interne werkzone die voldoet aan de voorwaarden van klasse A en die een ononderbroken, continue isolatie van de binnenzijde ten opzichte van de externe omgeving biedt"

Isolators hebben diverse toepassingen om aseptische processen te beschermen, waaronder:
- Luchtdichte/opblaasbare afdichtingen op alle deuren
- Vergrendelingen om te voorkomen dat deuren worden geopend nadat aseptische omstandigheden zijn bereikt (na biologische ontsmetting)
- Unidirectionele luchtstroming tussen 0,36-0,45 m/s (om te voldoen aan de richtlijnwaarden van EU GMP-bijlage 1)
- HEPA-filters om de binnenkomende lucht te zuiveren
- Drukverschillen, druktesten voor behuizing en handschoenen afzonderlijk
- Omgevingsmonitorsystemen om te bevestigen dat de omgeving aseptisch blijft tijdens gebruik
- Luchtstromings- en drukalarmen
- Waterstofperoxidedampsysteem voor bio-decontaminatie in patiëntenkamer en in het hele ziekenhuis het bereiken van een 6-log sporendodende werking* ter eliminatie van besmetting op de oppervlakken van de behuizing en binnenkomende materialen die nodig zijn voor het testproces
*Bij gebruik volgens de instructies op het etiket werken Ecolab Bioquell-systemen met het Bioquell waterstofperoxide-sterilisatiemiddel-AQ (EPA registratienummer:1677-277)
Voordelen van isolatoren
Isolatoren verkleinen in de eerste plaats het risico op vals positieve resultaten tijdens steriliteitstesten waardoor fabrikanten van steriele producten miljoenen dollars kunnen besparen, omdat onnodig afschrijven van producten tot een minimum wordt beperkt.
Een bijkomend voordeel is dat isolatoren ook kunnen zorgen voor aanzienlijke besparingen op de bedrijfskosten.
In tegenstelling van een biologische veiligheidskast (BSC)/laminaire airflowkast (LAF) die in een klasse B-cleanroom moeten worden geplaatst, kunnen isolatoren in een lagere klasse C/D-cleanroom worden geplaatst. Dit kan resulteren in aanzienlijke besparingen vanwege:
- Energierekeningen van een HVAC-systeem met een lagere capaciteit
- Minder arbeidskrachten (voor reiniging en desinfectie)
- Minder onderhoud van de cleanroom
- Lagere kosten voor schoonmaak- en desinfectieverbruiksartikelen
- Minder kledingvoorschriften
- Verhoogde efficiëntie van operators omdat ze met minder kledingvoorschriften langer kunnen doorwerken
1Kosten van een cleanroom per vierkante voet, cleanroomtechnologie, 28 februari 2018


Traditionele isolatoren van roestvrij staal in vergelijking met de Bioquell Qube